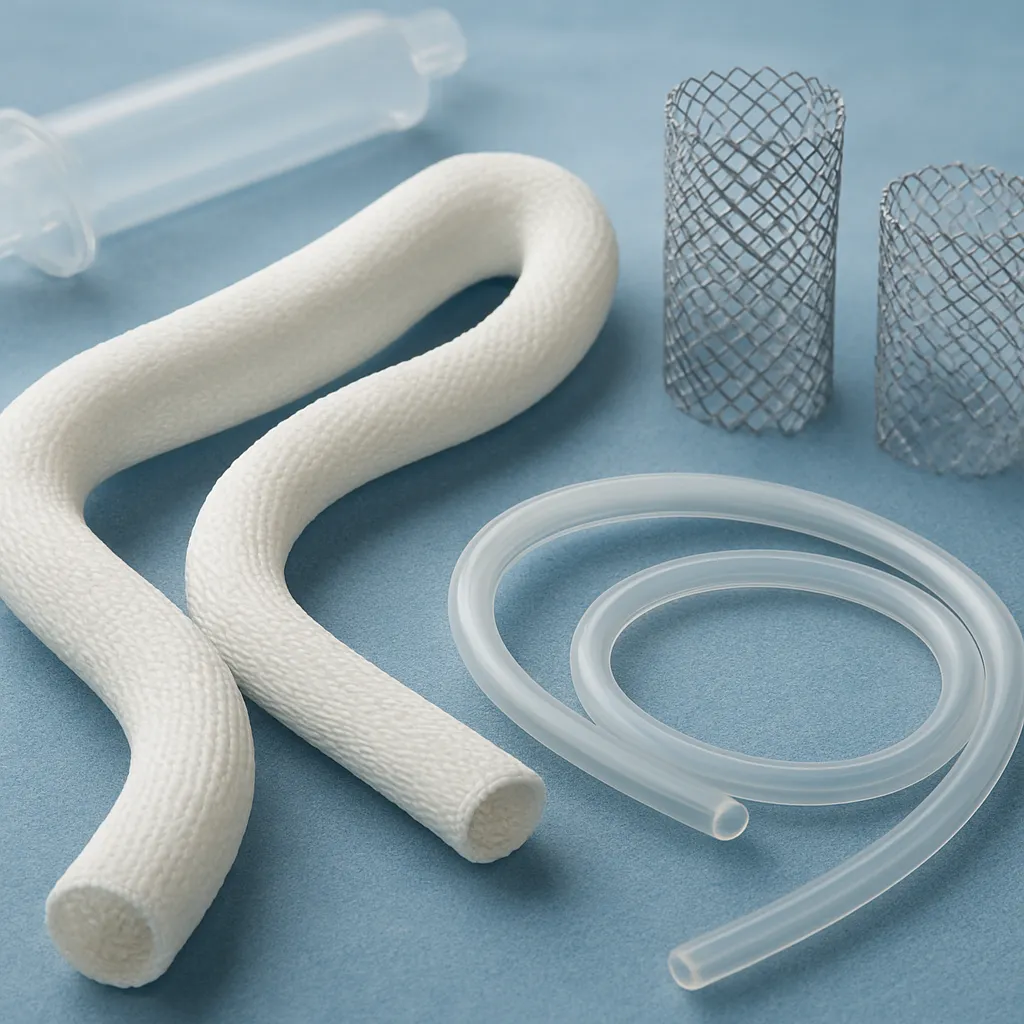
Rozwój protezy naczyniowej jako wyrobu medycznego był jednym z kluczowych osiągnięć współczesnej chirurgii naczyniowej i kardiochirurgii. Umożliwił leczenie tętniaków aorty, rozległych uszkodzeń tętnic oraz zaawansowanych zmian miażdżycowych, które wcześniej prowadziły do nieuchronnej amputacji lub zgonu. W centrum zainteresowania inżynierii biomedycznej znajdują się dziś przede wszystkim materiały biomedyczne, z których powstają wszczepy naczyniowe – to one decydują o trwałości, bezpieczeństwie i funkcjonalności protez. Od ich własności fizykochemicznych, biokompatybilności, odporności na zmęczenie i podatności na kolonizację bakteryjną zależy powodzenie zabiegów u setek tysięcy pacjentów rocznie. Wybór odpowiedniego materiału to zatem nie tylko problem techniczny, ale również zagadnienie o ogromnym znaczeniu klinicznym, ekonomicznym i etycznym dla całego przemysłu medycznego.
Kluczowe wymagania stawiane materiałom w protezach naczyniowych
Proteza naczyniowa musi jednocześnie wytrzymywać obciążenia hemodynamiczne, współpracować z żywą tkanką i zapewniać odpowiedni przepływ krwi przez wiele lat. Stawia to materiałom wymagania znacznie bardziej złożone niż w klasycznej inżynierii mechanicznej. Podstawowym parametrem jest oczywiście biokompatybilność, rozumiana jako zdolność materiału do długotrwałego kontaktu z krwią i ścianą naczynia bez wywoływania szkodliwej reakcji organizmu. Substancje uwalniane z materiału nie mogą być toksyczne, mutagenne, ani silnie prozapalne, a struktura powierzchni nie powinna sprzyjać nadmiernej aktywacji płytek krwi.
Drugą kategorią wymagań są właściwości mechaniczne. Proteza ma przejmować funkcję naczynia, zatem musi przenosić ciśnienie tętnicze rzędu 120–140 mmHg w warunkach ciągłych cykli skurczu i rozkurczu, a w niektórych lokalizacjach także działanie sił zginających, skręcających i ścinających. Istotne są:
- odporność na pękanie i zmęczenie,
- odporność na ścieranie wewnętrzne i uszkodzenia wskutek kontaktu z narzędziami chirurgicznymi,
- sprężystość pozwalająca na współpracę z natywnym naczyniem.
Kolejną grupą wymogów są parametry reologiczne i tekstylne – w przypadku protez tkanych lub dzianych. Stopień porowatości ściany protezy wpływa na przesiąkliwość, wnikanie komórek, szybkość wykrzepiania krwi w ścianie, a w dalszej perspektywie na proces ingrowth, czyli zarastania wszczepu tkanką. Nadmiernie porowaty materiał może prowadzić do przecieków krwi w okresie okołooperacyjnym, zbyt mało porowaty ogranicza integrację biologiczną i sprzyja tworzeniu się długoterminowego skrzepliny przyściennej.
Istotne są także aspekty technologiczne i logistyczne, które kształtują cały łańcuch dostaw w przemyśle medycznym. Materiał powinien dawać się łatwo sterylizować metodami powszechnie stosowanymi w szpitalach (para wodna, tlenek etylenu, promieniowanie gamma), umożliwiać precyzyjną obróbkę, składowanie i transport bez utraty własności. Ważna jest stabilność wymiarowa i odporność na starzenie się podczas wieloletniego przechowywania w magazynach producenta i odbiorców.
Z punktu widzenia klinicznego nie wolno pominąć wymagań związanych z trombogennością i potencjałem do endotelizacji. Idealny materiał powinien wspierać tworzenie cienkiej, fizjologicznej warstwy śródbłonka na wewnętrznej powierzchni protezy, co chroniłoby przed zakrzepicą i hiperplazją neointimy. Jest to szczególnie ważne w protezach o małej średnicy (tętnice wieńcowe, tętnice obwodowe), gdzie ryzyko zamknięcia przeszczepu jest najwyższe.
Wreszcie w kontekście systemowym pojawia się kwestia kosztów. Materiały nowej generacji – zaawansowane polimery bioaktywne, kompozyty, struktury hybrydowe – są często dużo droższe niż klasyczny poliester czy politetrafluoroetylen. Przemysł medyczny musi równoważyć oczekiwane korzyści kliniczne z realiami refundacji i budżetami systemów ochrony zdrowia, co przekłada się na decyzje o skalowaniu produkcji i wprowadzaniu nowych rozwiązań na rynek.
Tradycyjne materiały syntetyczne: poliester (Dacron) i PTFE
Najdłużej stosowaną grupą materiałów w protezach naczyniowych są tworzywa syntetyczne o ugruntowanej pozycji klinicznej: poliester (handlowo znany jako Dacron) oraz politetrafluoroetylen ekspandowany (ePTFE). Od kilkudziesięciu lat stanowią one podstawowy segment rynku dużych protez tętniczych, szczególnie w chirurgii aorty brzusznej i piersiowej oraz tętnic biodrowych i udowych.
Poliester (Dacron) – struktury tkane i dziane
Poliestrowe protezy naczyniowe wytwarza się techniką tkacką lub dziewiarską, co pozwala na formowanie protez rurowych, rozgałęzionych oraz specjalnych kształtek stosowanych np. w rekonstrukcji łuku aorty. Struktury tkane (woven) charakteryzują się mniejszą porowatością i lepszą szczelnością, co ogranicza krwawienie w czasie operacji, ale utrudnia wnikanie tkanek i komórek. Struktury dziane (knitted) są bardziej porowate, elastyczne, łatwiej dopasowują się do kształtu anatomicznego i sprzyjają integracji z otaczającą tkanką, jednak mogą wymagać wstępnego uszczelnienia.
Materiał poliestrowy jest stosunkowo łatwy w obróbce, dobrze znosi sterylizację parową i promieniowaniem, a jego trwałość mechaniczna została potwierdzona wieloletnimi obserwacjami klinicznymi. Protezy Dacronowe cechują się znaczną odpornością na rozciąganie i rozdarcie, co ułatwia manipulację podczas zabiegu chirurgicznego. Poliester jest jednak materiałem obojętnym biologicznie – nie ulega degradacji, ale też nie aktywnie wspiera procesów regeneracyjnych. Długoterminowo w ścianie protezy osadza się tkanka włóknista, a jej powierzchnia wewnętrzna pokrywa się warstwą neointimy.
Istnieją także warianty impregnowane, w których włókna poliestrowe pokrywa się substancjami uszczelniającymi, takimi jak kolagen, żelatyna lub albumina ludzkiego pochodzenia. Celem jest ograniczenie przesiąkania krwi na etapie implantacji. Z perspektywy przemysłowej taka modyfikacja oznacza konieczność wdrożenia dodatkowych procesów wytwórczych, kontroli jakości oraz walidacji biologicznej komponentów białkowych, ale pozwala na rozszerzenie portfolio produktów o wyroby dopasowane do różnych technik operacyjnych.
ePTFE – politetrafluoroetylen ekspandowany
Drugim filarem syntetycznych protez naczyniowych jest PTFE, a dokładniej jego odmiana ekspandowana (ePTFE). Powstaje poprzez rozciąganie politetrafluoroetylenu w kontrolowanych warunkach, co tworzy mikrostrukturalną sieć włókien i porów o określonej wielkości. Taka struktura zapewnia korzystny kompromis między szczelnością a możliwością wnikania komórek oraz sprzyja tworzeniu stabilnej neointimy.
PTFE jest materiałem o bardzo niskiej energii powierzchniowej i znakomitej odporności chemicznej. Słabo reaguje z otoczeniem, jest hydrofobowy i ma właściwości ślizgowe, dzięki czemu wewnętrzna powierzchnia protezy stawia stosunkowo niewielki opór przepływającej krwi. Z drugiej strony ta sama obojętność chemiczna utrudnia adhezję komórek śródbłonka, co ogranicza naturalną endotelizację. W zastosowaniach do dużych naczyń, takich jak aorta czy tętnice biodrowe, wyniki kliniczne ePTFE są jednak bardzo dobre, a materiał ten jest postrzegany jako niezwykle trwały.
W przemyśle medycznym protezy z ePTFE od lat stanowią istotny segment rynku zarówno w wersji klasycznej (otwarta chirurgia), jak i w formie stent-graftów do implantacji wewnątrznaczyniowej. Łączenie cienkościennej rury z ePTFE z metalowym szkieletem ze stali nierdzewnej lub stopu niklowo-tytanowego (Nitinol) pozwoliło na opracowanie systemów endowaskularnych do leczenia tętniaków bez otwierania jamy brzusznej czy klatki piersiowej. Wymagało to jednak dopracowania technologii łączenia różnoimiennych materiałów, odporności na zginanie oraz długotrwałej stabilności geometrii w zmiennym środowisku hemodynamicznym.
Ograniczenia syntetycznych materiałów tradycyjnych
Mimo wielu zalet klasyczne syntetyczne protezy naczyniowe mają wyraźne ograniczenia, szczególnie w naczyniach o małej średnicy, poniżej 6 mm. W tym zakresie znacząco rośnie ryzyko zakrzepicy i zwężenia przeszczepu. Wysoka trombogenność powierzchni polimerów, brak fizjologicznej warstwy śródbłonka oraz różnica sztywności między protezą a naczyniem natywnym sprzyjają zaburzeniom przepływu i lokalnym przeciążeniom ściany.
Problemy te doprowadziły do intensywnego rozwoju materiałów modyfikowanych, hybrydowych oraz biologicznych, a także do wdrożenia powłok przeciwzakrzepowych. Z perspektywy przemysłu medycznego oznacza to przejście od prostych, jednorodnych rur polimerowych do coraz bardziej złożonych wyrobów, w których materiał bazowy jest jedynie platformą dla powłok, cząsteczek czynnych i elementów nośnych.
Biologiczne i hybrydowe materiały w protezach naczyniowych
W odpowiedzi na ograniczenia protez syntetycznych powstała obszerna grupa rozwiązań wykorzystujących tkanki pochodzenia ludzkiego lub zwierzęcego, a także konstrukcje hybrydowe, łączące polimery z komponentami biologicznymi. Celem jest osiągnięcie lepszej integracji z organizmem, niższego ryzyka zakrzepicy i długotrwałej stabilności hemodynamicznej, przy jednoczesnym zachowaniu odporności mechanicznej.
Homografty i allografty naczyniowe
Homograftami (allograftami) naczyniowymi nazywa się fragmenty naczyń pobrane od zmarłych dawców ludzkich, odpowiednio przygotowane i przechowywane w bankach tkanek. Takie przeszczepy zachowują naturalną budowę ściany naczynia, w tym warstwę sprężystą i mięśniową, co w teorii powinno zapewniać znakomite właściwości hemodynamiczne i mechaniczne.
W praktyce stosowanie homograftów jest ograniczone z powodów logistycznych i immunologicznych. Dostępność odpowiednich dawców jest niewielka, proces pobierania, sterylizacji i przechowywania tkanek wymaga rozbudowanej infrastruktury banków tkanek, a procedury muszą spełniać rygorystyczne normy bezpieczeństwa biologicznego. Przemysł w tym przypadku koncentruje się bardziej na wspieraniu infrastruktury i dostarczaniu systemów konserwacji oraz przechowywania niż na masowej produkcji wszczepów.
Ksenoimplanty – materiały pochodzenia zwierzęcego
Znacznie większe możliwości przemysłowego wytwarzania stwarzają tkanki pochodzenia zwierzęcego, najczęściej świńskiego lub bydlęcego. Mogą to być fragmenty osierdzia, ściany naczyniowej lub specjalnie preparowane matryce kolagenowe. Kluczowym etapem jest usunięcie komórek (decelularyzacja) oraz stabilizacja struktury białkowej chemicznymi środkami sieciującymi, takimi jak glutaraldehyd.
Powstałe w ten sposób protezy biologiczne łączą naturalną architekturę macierzy pozakomórkowej z możliwością kolonizacji przez komórki gospodarza. W założeniu mają stopniowo integrować się z tkankami pacjenta, a nawet częściowo przebudowywać w kierunku struktury zbliżonej do naczynia natywnego. W praktyce ich zastosowanie jest jak dotąd ograniczone głównie do specyficznych wskazań, m.in. w chirurgii dziecięcej czy rekonstrukcji naczyń zakażonych, gdzie syntetyczne materiały wypadają słabiej.
Z industrialnego punktu widzenia produkcja ksenoimplantów wymaga utrzymania ściśle kontrolowanych łańcuchów dostaw materiału surowego, monitorowania stad zwierząt, zapewnienia pełnej identyfikowalności i nadzoru nad chorobami odzwierzęcymi. Wymaga to ścisłej współpracy producentów z sektorem weterynaryjnym i regulatorem, a także zaawansowanych procesów oczyszczania i walidacji biologicznej.
Materiały hybrydowe – połączenie polimerów i tkanki
Trzecią grupą w obrębie biomateriałów biologicznych są konstrukcje hybrydowe, w których syntetyczny szkielet polimerowy (np. poliester) stanowi rusztowanie dla nasączonej lub nałożonej tkanki biologicznej. Przykładem może być proteza poliestrowa powleczona osierdziem bydlęcym lub zewnętrzna siatka polimerowa otaczająca biologiczny rdzeń naczyniowy.
Takie podejście pozwala połączyć wytrzymałość mechaniczną i powtarzalność wymiarową syntetyku z potencjalnie lepszą biokompatybilnością powierzchni biologicznej. Z punktu widzenia przemysłu medycznego konstrukcje hybrydowe są bardziej złożone technologicznie: wymagają synchronizacji procesów polimerowych i biologicznych, wieloetapowej kontroli jakości oraz złożonej dokumentacji regulacyjnej. Jednocześnie umożliwiają tworzenie produktów wysoko wyspecjalizowanych, przeznaczonych do trudnych przypadków klinicznych, co często uzasadnia ich wyższą cenę.
Ryzyka i wyzwania związane z materiałami biologicznymi
Choć materiały biologiczne i hybrydowe oferują liczne potencjalne korzyści, wiążą się także z istotnymi wyzwaniami. Jednym z głównych problemów jest możliwość degradacji i zwapnienia w długiej perspektywie czasowej. Protezy oparte na kolagenie mogą ulegać sztywnieniu, pogrubieniu ściany i utracie elastyczności, co pogarsza ich parametry hemodynamiczne. U dzieci dochodzi do tego problem braku wzrostu wraz z organizmem – zastąpione naczynie biologiczne zwykle nie ma zdolności do fizjologicznego poszerzania się w miarę dojrzewania pacjenta.
Nie można również pominąć ryzyka immunologicznego. Choć nowoczesne technologie decelularyzacji znacząco ograniczają obecność obcych antygenów, u części pacjentów może dochodzić do przewlekłej reakcji zapalnej, przyspieszonej degeneracji wszczepu lub jego zakrzepicy. Dlatego producenci są zobowiązani do prowadzenia długoterminowych badań klinicznych, monitorowania efektów poimplantacyjnych i aktualizacji dokumentacji bezpieczeństwa zgodnie z wymogami regulatorów.
Nowe trendy: modyfikacje powierzchni, powłoki bioaktywne i inżynieria tkankowa
Rozwój nauk materiałowych, chemii powierzchni i biologii komórki otworzył drogę do kolejnej generacji materiałów naczyniowych. Coraz rzadziej mamy do czynienia z „gołą” rurą polimerową; częściej jest to złożona konstrukcja, w której dużą rolę odgrywają powłoki, mikroteksturowanie oraz integracja substancji bioaktywnych. Jednocześnie dynamicznie rozwija się dziedzina zbliżająca protezy naczyniowe do tzw. inżynieria tkankowa.
Powłoki przeciwzakrzepowe i modyfikacje chemiczne
Jednym z najważniejszych kierunków jest wprowadzanie na powierzchnię protez cząsteczek o działaniu antykoagulacyjnym lub antyagregacyjnym. Klasycznym przykładem są powłoki oparte na heparynie. Cząsteczki heparyny są chemicznie lub fizycznie wiązane z powierzchnią ePTFE albo poliestru, co ma ograniczać aktywację kaskady krzepnięcia i tworzenie zakrzepów na wczesnym etapie po implantacji.
Inne strategie obejmują:
- modyfikację powierzchni polimeru tak, aby była bardziej hydrofilowa i sprzyjała tworzeniu cienkiej warstwy białek osocza w konformacji mniej aktywującej płytki,
- wiązanie peptydów adhezyjnych (np. fragmentów sekwencji RGD) stymulujących zasiedlanie protezy przez komórki śródbłonka,
- powlekanie cienkimi warstwami tlenków metali o korzystnym profilu interakcji z krwią.
Implementacja takich technologii w przemyśle wymaga zaawansowanych linii produkcyjnych, łączących procesy chemiczne, plazmowe lub osadzanie warstw w próżni z tradycyjną obróbką polimerów. Każda dodatkowa powłoka oznacza też konieczność potwierdzenia jej stabilności, równomiernego rozkładu i braku toksyczności produktów degradacji, co znacząco wydłuża i komplikuje proces dopuszczania wyrobu do obrotu.
Bioaktywne matryce i kontrolowane uwalnianie substancji
Kolejnym krokiem jest nadanie protezom właściwości czynnych – zdolności do kontrolowanego uwalniania leków i związków biologicznie aktywnych. W ściankę protezy można wbudować np. leki przeciwproliferacyjne (hamujące przerost błony wewnętrznej) lub czynniki wzrostu wspierające angiogenezę i reendotelializację. Stosuje się w tym celu cienkie warstwy polimerów biodegradowalnych, takich jak poli-L-mlekowy (PLLA) czy kopolimery PLA/PGA, w których zamknięto odpowiednie substancje.
Wymaga to precyzyjnego zaprojektowania kinetyki degradacji nośnika oraz dyfuzji leku, tak aby jego stężenie w ścianie protezy było optymalne w krytycznym okresie gojenia naczynia. Z perspektywy przemysłowej łączy to wyzwania klasycznej produkcji protez z wymaganiami właściwymi dla produktów leczniczych, co skutkuje koniecznością spełnienia kryteriów zarówno wyrobu medycznego, jak i lekowego (tzw. wyroby medyczne z funkcją pomocniczą leku).
Scaffolding i protezy „hodowane” z komórek pacjenta
Najbardziej zaawansowanym nurtem rozwoju są protezy tworzone w oparciu o rusztowania (scaffolds), które zasiedla się komórkami pacjenta lub komórkami allogenicznymi przed implantacją. Materiałem bazowym rusztowania mogą być zarówno polimery syntetyczne (PLLA, PCL, poliuretany), jak i matryce kolagenowe lub kompozyty. Kluczowe jest zapewnienie odpowiedniej mikroarchitektury porów, która pozwoli na migrację komórek, tworzenie sieci naczyń mikrokrążenia oraz odkładanie macierzy pozakomórkowej.
Takie „żywe” protezy mogą mieć zdolność do remodelingu i adaptacji do zmieniających się warunków hemodynamicznych, a w idealnym scenariuszu także do wzrostu wraz z organizmem. Z technicznego punktu widzenia łączy się tu procesy typowe dla przemysłu medycznego z metodami biotechnologicznymi: hodowlą komórkową, stosowaniem bioreaktorów, kontrolą warunków fizjologicznych i sterylnych. Koszt jednostkowy takich wyrobów jest obecnie bardzo wysoki, a produkcja często ma charakter indywidualny lub małoseryjny.
Dalszy rozwój tego segmentu zależy więc od postępu w automatyzacji procesów hodowli komórek, standaryzacji bioreaktorów oraz uregulowania kwestii prawnych związanych z produktami inżynierii tkankowej. W dłuższej perspektywie może on jednak zrewolucjonizować sposób, w jaki rozumiemy pojęcie „materiału” w protezie naczyniowej, przesuwając akcent z obojętnego tworzywa na dynamiczny, współtworzony przez organizm wszczep.
Druk 3D i personalizacja geometrii
Istotnym trendem jest zastosowanie technologii przyrostowych (druk 3D) do tworzenia indywidualnie dopasowanych protez naczyniowych i stent-graftów. Choć sam materiał może być zbliżony do już stosowanych polimerów, kluczową nowością jest możliwość idealnego odtworzenia anatomicznego przebiegu i średnicy naczynia na podstawie danych obrazowych (tomografia komputerowa, rezonans magnetyczny).
Dla przemysłu oznacza to konieczność zmiany modelu produkcyjnego: z dużych serii standardowych protez na elastyczne linie wytwórcze zdolne do szybkiego wytwarzania małoseryjnych, spersonalizowanych wyrobów. Materiał, aby sprawdzić się w druku 3D, musi wykazywać odpowiednie właściwości reologiczne, możliwość sterylizacji oraz stabilność wymiarową po procesie wydruku. Coraz większe znaczenie mają również certyfikowane granulaty i żywice medyczne kompatybilne z konkretnymi technologiami przyrostowymi.